Headline
Warga AS menolak kepemimpinan yang kian otoriter.
 Kumpulan Berita DPR RI
Kumpulan Berita DPR RI
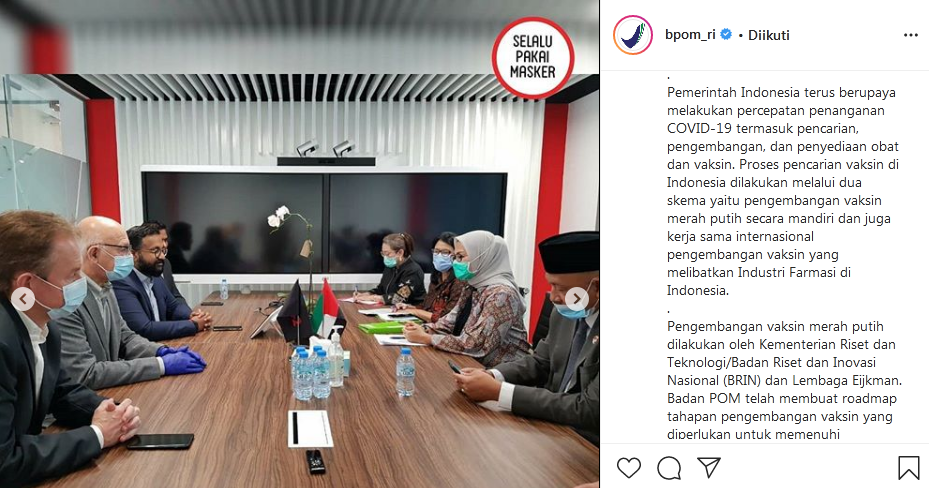
KEPALA Badan Pengawas Obat dan Makanan (Badan POM) Republik Indonesia Penny K Lukito mendatangi Uni Emirat Arab (UEA) yang tengah melakukan uji klinis Fase III vaksin korona buatan BUMN Tiongkok, Sinopharm.
Dalam kunjungan ke UEA, Kepala Badan POM melakukan serangkaian pertemuan dengan Assistant Undersecretary of Health Policy and Licensing of UAE Ministry of Health (Kementerian Kesehatan UEA) Dr Amin Hussain Al Amiri, Acting Undersecretary of Abu Dhabi Department of Health (DoH) Dr Jamal Alkaabi, CEO Group-42 (G-42) Mr Peng Xiao, Sinopharm serta mengunjungi Vaccine Testing Centre yang berlokasi di Abu Dhabi National Exhibition Centre.
“Kunjungan ini bertujuan khususnya untuk memberikan dukungan langkah-langkah regulatori dalam rangka mengakselerasi akses vaksin COVID-19 dan mendapatkan informasi data terkait pelaksanaan uji klinis yang saat ini tengah dalam proses fase 3 di UEA,” jelas Penny seperti dilansir dari laman Badan POM, Selasa (1/9).
Pada kunjungan tersebut, kata Penny, ia mendapati beberapa aspek-aspek positif dalam pelaksanaan uji klinis tahap ketiga di UEA yang ditargetkan untuk diikuti oleh 22.000 peserta itu. Lebih dari 100 dokter dan tenaga farmasi, 1.000 perawat dan petugas laboratorium terlibat dalam uji klinis.
Menurut Penny, G-42 memandang keragaman populasi ini akan memberikan hasil uji klinis yang valid. Keikutsertaan pimpinan tertinggi UEA di awal uji klinis kandidat vaksin covid-19, dapat mendorong masyarakat untuk secara sukarela menjadi peserta uji klinis, sampai saat ini dari target seluruhnya 22.000 subjek, sudah dapat direkrut 15.000 subjek.
“Kami meninjau langsung pelaksanaan uji klinis vaksin COVID-19 di Vaccine Testing Centre. Hal ini dilakukan untuk memastikan uji klinis tersebut dijalankan dengan baik dan sesuai dengan ketentuan untuk mendukung data keamanan dan khasiat vaksin tersebut,” jelas Kepala Badan POM.
Kandidat vaksin covid-19 ini telah mendapatkan Emergency Use Authorization (EUA) dari Regulator Pengawas Obat Republik Rakyat Tiongkok (RRT), yaitu National Medicines Products Administration (NMPA) pada Juli 2020 berdasarkan hasil uji klinis fase 1 dan 2 dan telah mendapatkan sertifikasi halal. Hasil uji klinis tersebut juga telah dipublikasi di JAMA (The Journal of American Medical Association).
Dalam pertemuan dengan CEO Group-42 (G-42) Peng Xiao, juga dibahas adanya kesempatan bagi industri farmasi di Indonesia untuk menjadi bagian dalam proses transfer teknologi produksi vaksin tersebut, yang dapat digunakan baik untuk di Indonesia maupun di ekspor ke negara lain. Hal tersebut disambut baik, mengingat saat ini kesiapan industri vaksin di UEA belum tersedia dalam waktu dekat.
"Dialog dan kerja sama antara Badan POM dan Kemkes UEA akan sangat bermanfaat untuk memastikan akses yang cepat atas vaksin tesebut melalui proses regulatori yang terarah dan sejalan dengan standar internasional. Hal ini akan mendorong percepatan pemberian EUA tepat pada waktunya," kata Penny.
Kedua lembaga sepakat untuk menuangkan dukungan kolaborasi dalam bentuk Memorandum of Understanding (MoU) sebagai platform untuk mengawal proses regulasi di bidang obat dan vaksin dan kerja sama untuk pengembangan industri farmasi di kedua negara.
Khusus untuk pengembangan vaksin covid-19 dalam rangka menyediakan kapasitas produksi komersial yang besar, terdapat peluang menggunakan sarana produksi Bio Farma, mengingat saat ini di UEA sedang dalam taraf pembangunan industri vaksin. Pemerintah UEA mengharapkan adanya kerja sama yang saling menguntungkan (mutual benefit) untuk mengawal ketersediaan vaksin yang aman, berkualitas, dan efektif di kedua negara.
Kepala Badan POM UEA Amin Hussain Al Amiri menaruh apresiasi yang tinggi kepada Indonesia terhadap komitmen kuat antara pejabat tinggi kedua negara dalam mendukung kolaborasi untuk mengembangkan vaksin covid-19 dalam memenuhi kebutuhan Indonesia.
Sebagai langkah awal kerja sama, kedua regulator sepakat untuk melakukan joint assessment serta sharing data terkait assessment report vaccine dari Sinopharm yang rencananya akan disampaikan oleh G-42 pada bulan September atau Oktober 2020, hal tersebut dapat mempercepat proses evaluasi terhadap data khasiat, keamanan, dan mutu vaksin dari Sinopharm.
"Kerja sama ini dapat menguntungkan Indonesia dalam segi memenuhi kebutuhan vaksin COVID-19 dan membuka peluang industri farmasi Indonesia melakukan ekspor obat dan vaksin Indonesia ke negara-negara Timur Tengah melalui UEA sebagai hub sekaligus mendorong implementasi Rencana Aksi OKI untuk mendukung kemandirian obat dan vaksin di negara anggota OKI," pungkas Penny.
Kunjungan Kepala Badan POM ini menindaklanjuti pertemuan pada 19-21 Agustus 2020 lalu yang dilakukan oleh Menteri Luar Negeri RI Retno Marsudi dan Menteri Badan Usaha Milik Negara (BUMN) RI Erick Thohir ke Tiongkok dan UEA. Kunjungan tersebut berhasil mendapatkan komitmen UEA untuk menyediakan 10 juta vaksin covid-19 untuk Indonesia melalui kerja sama antara perusahaan G-42, UEA dengan Sinopharm, Tiongkok dan Kimia Farma. (Fer/H-2)
Presiden Prabowo terima Menteri Keamanan Tiongkok Chen Yi Xin di Istana Negara. Bahas penguatan kerja sama keamanan dan intelijen BIN-MSS demi stabilitas kawasan.
Ilmuwan Tiongkok menemukan waktu paling aman bagi manusia untuk beraktivitas di Bulan. Dengan suhu ekstrem dan radiasi tinggi, pemilihan waktu jadi kunci bertahan hidup.
Masa pensiun ISS mendekat pada 2030, namun stasiun ruang angkasa komersial penggantinya belum siap. AS hadapi risiko keamanan nasional dan persaingan ketat dengan Tiongkok.
Beijing dengan tegas menentang penggunaan kekuatan dalam hubungan internasional.
Dalam konflik yang terjadi selama Ramadan, Iran disebut memperoleh dukungan dari kedua negara tersebut, meskipun Beijing menyatakan sikap netral.
Komandan Shenzhou 21, Zhang Lu, baru saja mengukir sejarah sebagai astronaut Tiongkok dengan aktivitas luar kendaraan (EVA) terbanyak. Simak detail misinya!
Ia menegaskan jika tidak diawasi dengan baik peredaran obat ini berisiko memicu resistensi anti mikroba yang berdampak luas bagi kesehatan masyarakat.
BPOM melakukan pengawasan terhadap pangan takjil melalui pengujian cepat menggunakan rapid test kit, 108 sampel (2%) tidak memenuhi syarat.
Pengawasan ini merupakan upaya preventif pemerintah daerah dalam melindungi kesehatan publik selama bulan suci.
BPOM perketat pengawasan Program Makan Bergizi Gratis karena risiko keamanan pangan. Sepanjang 2024 tercatat 138 KLB keracunan.
BPOM mengajak masyarakat menjadi konsumen cerdas dan berdaya dengan selalu menerapkan Cek KLIK (Kemasan, Label, Izin edar, dan Kadaluarsa) sebelum membeli atau mengonsumsi produk pangan.
BPOM mencatat, suplemen ilegal dapat berasal dari pabrik-pabrik tersembunyi yang beroperasi di tengah permukiman padat dengan kondisi yang jauh dari standar Cara Pembuatan yang Baik (CPB).
Copyright @ 2026 Media Group - mediaindonesia. All Rights Reserved